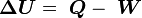Sendo K uma constante característica do material denominada condutividade térmica.

Lei de Fourier
Conduc_1.gif (2406 bytes)
Consideremos um elemento da barra de comprimento dx e secção S. A energia que entra no elemento de volume na unidade de tempo é JS, e a que sai é J’S. A energia do elemento varia, na unidade de tempo, de uma quantidade igual a diferença entre o fluxo entra e o fluxo que sai.
Esta energia, é empregada para mudar a temperatura do elemento. A quantidade de energia absorvida ou cedida (na unidade de tempo) pelo elemento é igual ao produto da massa deste elemento pelo calor específico e pela variação de temperatura.
Igualando ambas as expressões, e tendo em conta a lei de Fourier, obtemos a equação diferencial que descreve a condução térmica
Solução analítica
Suponhamos uma barra metálica de comprimento L, conectada por seus extremos a duas fontes de calor a temperaturas Ta e Tb respectivamente. Seja T0 a temperatura inicial da barra quando conectamos as fontes aos extremos da barra.
Ao cabo de certo tempo, teoricamente infinito, que na prática depende do tipo de material que empregamos, é estabelecido o estado estacionário no qual a temperatura de cada ponto da barra não varia com o tempo. Este estado é caracterizado por um fluxo J constante de energia. A lei de Fourier estabelece que a temperatura variará linearmente com a distância x a origem da barra.
Para descrever o estado transitório buscamos uma solução da forma T(x, t)=F(x)·G(t), variáveis separadas
O sinal negativo assegura o caráter transitório.
Integramos a primeira equação diferencial
Integramos a segunda equação diferencial
É uma equação diferencial similar a de um MHS, cuja solução é a·sen(ωr+δ)
A temperatura em qualquer ponto x ao longo da barra, em um instante determinado, T(x, t) é a solução da equação diferencial, que é uma combinação de dois termos, o que corresponde ao regime permanente mais o do regime transitório.
Condições de contorno
Em x=0, T(0, t)=Ta, temperatura fixa do extremo esquerdo da barra
Em x=L, T(L, t)=Tb, temperatura fixa do extremo direito da barra
O regime variável geral de temperaturas da barra é
Distribuição inicial de temperaturas
Somente, resta por determinar os coeficientes an, identificando esta solução com a distribuição inicial de temperaturas na barra T(x, 0)=T0 no instante t=0.
Mais abaixo, são proporcionados os detalhes do cálculo dos coeficientes an do desenvolvimento em série ao leitor interessado.
A temperatura em qualquer ponto da barra x, em um instante t, é composta da soma de um termo proporcional a x, e de uma série rapidamente convergente que descreve o estado transitório.
O valor de α=K/(ρc) nos da uma medida da rapidez com a qual o sistema alcança o estado estacionário. Quanto maior seja α mais rápido é alcançado o estado estacionário
Atividades
Neste programa, estudaremos a condução do calor ao longo de uma barra metálica cujos extremos estão conectados a duas fontes de calor que tem distintas temperaturas. Observaremos a evolução da temperatura de cada ponto da barra a medida que transcorre o tempo.
Examinaremos os fatores que determinam a condução do calor ao longo de uma barra metálica, provando barras de distintos materiais, com distintas temperaturas fixas dos extremos e inicial da barra.
* Selecione no controle de seleção o Metal da barra. As unidades das grandezas estão expressas no Sistema Internacional de Unidades de Medida.
Metal Densidade Calor específico Condutividade térmica
α
Alumínio 2700 880 209.3 8.81·10-5
Aço 7800 460 45 1.25·10-5
Cobre 8900 390 389.6 11.22·10-5
Latão 8500 380 85.5 2.65·10-5
Prata 10500 230 418.7 17.34·10-5
Chumbo 11300 130 34.6 2.35·10-5
Foente: Koshkin N. I., Shirkévich M. G.. Manual de Física Elemental. Editorial Mir 1975. págs 36, 74-75, 85-86
Introduza, movendo as flechas de cor azul com o ponteiro do mouse
* A temperatura fixa no extremo esquerdo da barra Ta.
* A temperatura fixa no extremo direito da barra Tb.
* A temperatura inicial da barra T0.
* O comprimento da barra metálica foi fixado no valor de L=0.5 m.